La medicina del futuro
admin2023-02-09T14:52:43+01:00La Medicina del futuro
Farmacogenetica e Farmacogenomica possono essere considerate oggi la “Medicina di precisione” [Ritchie, Marylyn D; 2012]: in altri termini la Medicina non sarà più focalizzata, come è stato storicamente, sulla gestione della sintomatologia della malattia e su regimi terapeutici empirici, ma sarà rivolta verso una terapia individuale specifica basata sul patrimonio genetico del paziente [Wilke, Russell A et al. 2007]; questo perché, alcuni pazienti possono avere esperienze di reazioni avverse (ADR) che non si verificano in altri che assumono lo stesso farmaco allo stesso dosaggio. In passato le differenze nel rapporto rischio/beneficio di un farmaco tra i pazienti venivano attribuiti a tutta una serie di fattori come, l’età, il sesso, lo stato nutrizionale, le condizioni di salute generali, lo stile di vita (dieta, alcol fumo), eventuali terapie concomitanti etc , oggi invece in aggiunta a questi fattori, la variabilità genetica è stata riconosciuta come un ruolo fondamentale nella risposta individuale al trattamento. Studi su gemelli mono- e di-zigotici hanno mostrato come i fattori genetici influiscano nella maggior parte dei processi farmacocinetici e farmacodinamici [Mini, Enrico et al. 2009]. Le conseguenze cliniche della variabilità interindividuale nella risposta farmacologica possono essere quindi rappresentate da un fallimento terapeutico (mancato o parziale effetto della terapia ), da effetti collaterali di un determinato principio attivo o da reazioni avverse anche gravi e talvolta fatali.
Enzimi e Biochimica: una storia parallela
 Il termine “enzima” fu coniato nel 1878 da Fredrich Wilhelm Kuhne, per dimostrare che nel lievito vi fosse qualcosa che innescava reazioni della fermentazione. Successivamente, nel 1897, Eduard Buchner ottenne un estratto cellulare che poteva sintetizzare l’etanolo a partire da glucosio (fermentazione alcolica). Emil Fischer, nel 1894, portò alla formulazione della teoria della chiave e serratura, ovvero la specificità di un enzima (la serratura) per il suo substrato (la chiave) che deriva dalle loro forme geometriche complementari. James Sumner, nel 1926, riuscì a cristallizzare per la prima volta l’enzima ureasi, che catalizza l’idrolisi dell’urea in ammoniaca e anidride carbonica, dimostrando che questi cristalli contenevano una proteina. La grande varietà di reazioni biochimiche che cooperano al mantenimento della vita sono praticamente tutte mediate da una serie di proteine che svolgono una funzione biologica specifica fondamentale, gli enzimi. Le funzioni più importanti di queste molecole si basano sulla velocità di reazione. Le reazioni catalizzate possono avvenire in condizioni particolari di pH, temperatura e pressione, ma soprattutto hanno un elevato grado di specificità nei confronti dei loro substrati. L’inizio della storia dell’Enzimologia coincide con la storia della Biochimica stessa: in pratica queste due discipline si sono evolute insieme. Gli studi sulla fermentazione di Joseph Gay-Lussac, nel 1810, stabilirono che l’etanolo e la CO2 erano i principali prodotti della decomposizione dello zucchero da parte del lievito e, successivamente, nel 1835, Jacob Berzelius, nella prima teoria sulla catalisi chimica, stabilì che un estratto di malto, conosciuto oggi come diastasi, conteneva l’enzima α-amilasi, che catalizzava l’idrolisi dell’amido.
Il termine “enzima” fu coniato nel 1878 da Fredrich Wilhelm Kuhne, per dimostrare che nel lievito vi fosse qualcosa che innescava reazioni della fermentazione. Successivamente, nel 1897, Eduard Buchner ottenne un estratto cellulare che poteva sintetizzare l’etanolo a partire da glucosio (fermentazione alcolica). Emil Fischer, nel 1894, portò alla formulazione della teoria della chiave e serratura, ovvero la specificità di un enzima (la serratura) per il suo substrato (la chiave) che deriva dalle loro forme geometriche complementari. James Sumner, nel 1926, riuscì a cristallizzare per la prima volta l’enzima ureasi, che catalizza l’idrolisi dell’urea in ammoniaca e anidride carbonica, dimostrando che questi cristalli contenevano una proteina. La grande varietà di reazioni biochimiche che cooperano al mantenimento della vita sono praticamente tutte mediate da una serie di proteine che svolgono una funzione biologica specifica fondamentale, gli enzimi. Le funzioni più importanti di queste molecole si basano sulla velocità di reazione. Le reazioni catalizzate possono avvenire in condizioni particolari di pH, temperatura e pressione, ma soprattutto hanno un elevato grado di specificità nei confronti dei loro substrati. L’inizio della storia dell’Enzimologia coincide con la storia della Biochimica stessa: in pratica queste due discipline si sono evolute insieme. Gli studi sulla fermentazione di Joseph Gay-Lussac, nel 1810, stabilirono che l’etanolo e la CO2 erano i principali prodotti della decomposizione dello zucchero da parte del lievito e, successivamente, nel 1835, Jacob Berzelius, nella prima teoria sulla catalisi chimica, stabilì che un estratto di malto, conosciuto oggi come diastasi, conteneva l’enzima α-amilasi, che catalizzava l’idrolisi dell’amido.  Comunque, la natura proteica degli enzimi non fu generalmente accettata fino alla metà degli anni ‘30, quando John Northrop e Moses Kunitz stabilirono che esisteva una correlazione diretta tra l’attività della pepsina, della tripsina e della chimotripsina, tutte in forma cristallina, e la quantità di proteina presente. L’esperienza enzimologica ha poi dimostrato che gli enzimi sono proteine. Nel 1963 fu resa nota la prima sequenza aminoacidica di un enzima, la ribonucleasi A del pancreas bovino e nel 1965 si ottenne, sempre per la prima volta, una struttura a raggi X di un enzima, cioè del lisozima dell’albume dell’uovo. Da allora sono stati purificati circa 2.000 enzimi, numero che sta sempre comunque sempre crescendo. Nei primi anni ’80 sono stati scoperti alcuni esempi di catalisi biologica mediata da molecole di ribonucleasi batterica, coinvolta nel processo di trascrizione di tRNA (gli introni presenti nel trascritto primario di alcuni mRNA e rRNA sono ribozimi che possono catalizzare il processo di auto-splicing). Anche nella sintesi proteica la reazione della peptidil-transferasi è catalizzata da rRNA 23S della subunità 50S dei ribosomi. Per citare ancora altre molecole straordinarie gli “abzimi” sono anticorpi che possiedono attività catalitica, scoperti in malattie autoimmunitarie come la Sclerosi multipla, per la graduale distruzione della guaina mielinica che circonda i neuroni in cervello e midollo spinale: il siero di questi pazienti contiene anticorpi (di fatto proteasi) capaci di distruggere proteoliticamente la proteina basica della mielina. Anche nell’Emofilia A il disturbo della coagulazione è dovuto alla carenza del fattore VIII. Il siero di pazienti emofilici contiene anticorpi con attività proteolitica contro il fattore VIII.
Comunque, la natura proteica degli enzimi non fu generalmente accettata fino alla metà degli anni ‘30, quando John Northrop e Moses Kunitz stabilirono che esisteva una correlazione diretta tra l’attività della pepsina, della tripsina e della chimotripsina, tutte in forma cristallina, e la quantità di proteina presente. L’esperienza enzimologica ha poi dimostrato che gli enzimi sono proteine. Nel 1963 fu resa nota la prima sequenza aminoacidica di un enzima, la ribonucleasi A del pancreas bovino e nel 1965 si ottenne, sempre per la prima volta, una struttura a raggi X di un enzima, cioè del lisozima dell’albume dell’uovo. Da allora sono stati purificati circa 2.000 enzimi, numero che sta sempre comunque sempre crescendo. Nei primi anni ’80 sono stati scoperti alcuni esempi di catalisi biologica mediata da molecole di ribonucleasi batterica, coinvolta nel processo di trascrizione di tRNA (gli introni presenti nel trascritto primario di alcuni mRNA e rRNA sono ribozimi che possono catalizzare il processo di auto-splicing). Anche nella sintesi proteica la reazione della peptidil-transferasi è catalizzata da rRNA 23S della subunità 50S dei ribosomi. Per citare ancora altre molecole straordinarie gli “abzimi” sono anticorpi che possiedono attività catalitica, scoperti in malattie autoimmunitarie come la Sclerosi multipla, per la graduale distruzione della guaina mielinica che circonda i neuroni in cervello e midollo spinale: il siero di questi pazienti contiene anticorpi (di fatto proteasi) capaci di distruggere proteoliticamente la proteina basica della mielina. Anche nell’Emofilia A il disturbo della coagulazione è dovuto alla carenza del fattore VIII. Il siero di pazienti emofilici contiene anticorpi con attività proteolitica contro il fattore VIII.
Le reazioni biochimiche avvengono in condizioni “speciali” per i valori di temperatura, pressione e pH fisiologico: la maggior parte delle reazioni che si verificano nelle cellule sarebbero estremamente lente e gli enzimi sono infatti catalizzatori biologici, cioè hanno il potere di accelerare enormemente le reazioni chimiche tipiche dei processi vitali. Una particolarità di molti enzimi è inoltre la “stereospecificità”, essendo attivi su uno solo di due enantiomeri; altri, anche se dotati di specificità meno stretta, agiscono solo su molecole molto simili e lo fanno comunque con affinità e velocità diverse (in pratica: modulazione fisiologica). La cristallografia ai raggi x viene utilizzata per determinare la forma molecolare di un enzima con e senza substrato legato al sito attivo: gli enzimi quindi, in condizioni favorevoli, possono elaborare substrati specie-specifici per le cellule, in una sorta di moto perpetuo e sequenziale.
Da qui la rivoluzionaria svolta della Enzimologia biodinamica, definita a buon diritto “paradigma di ogni strategia medica” [Lenzi S.; 2016].















 Esse hanno movimenti di diffusione laterale così veloci che una molecola può circumnavigare un eritrocita in pochi secondi. Il grado di fluidità dipende dalla composizione lipidica e dalla temperatura; a bassa temperatura i movimenti sono molto limitati e il doppio strato è una struttura quasi cristallina (paracristallina). Sopra una certa temperatura che è caratteristica per ogni tipo di membrana, i lipidi possono muoversi liberamente e velocemente; la temperatura di transizione da uno stato paracristallino solido a quello fluido dipende dalla composizione lipidica della membrana. Gli acidi grassi saturi si impacchettano bene nelle strutture paracristalline, mentre i ripiegamenti nelle catene di acidi grassi insaturi interferiscono con l’impacchettamento e impediscono la formazione di uno strato paracristallino: più elevata è la proporzione di acidi grassi saturi, più elevata è la temperatura di transizione solido-fluido della membrana. Il contenuto in steroli è un altro determinante della temperatura di transizione di una membrana; la struttura rigida e planare del nucleo steroideo inserita fra la catena degli acidi grassi produce due effetti sulla fluidità: sotto la temperatura di transizione solido-fluido l’inserzione dello sterolo impedisce una disposizione altamente ordinata
Esse hanno movimenti di diffusione laterale così veloci che una molecola può circumnavigare un eritrocita in pochi secondi. Il grado di fluidità dipende dalla composizione lipidica e dalla temperatura; a bassa temperatura i movimenti sono molto limitati e il doppio strato è una struttura quasi cristallina (paracristallina). Sopra una certa temperatura che è caratteristica per ogni tipo di membrana, i lipidi possono muoversi liberamente e velocemente; la temperatura di transizione da uno stato paracristallino solido a quello fluido dipende dalla composizione lipidica della membrana. Gli acidi grassi saturi si impacchettano bene nelle strutture paracristalline, mentre i ripiegamenti nelle catene di acidi grassi insaturi interferiscono con l’impacchettamento e impediscono la formazione di uno strato paracristallino: più elevata è la proporzione di acidi grassi saturi, più elevata è la temperatura di transizione solido-fluido della membrana. Il contenuto in steroli è un altro determinante della temperatura di transizione di una membrana; la struttura rigida e planare del nucleo steroideo inserita fra la catena degli acidi grassi produce due effetti sulla fluidità: sotto la temperatura di transizione solido-fluido l’inserzione dello sterolo impedisce una disposizione altamente ordinata
 I domini carbossiterminali e amminoterminale contengono molti residui amminoacidici polari o carchi e sono quindi relativamente idrofilici; un lungo segmento al centro della molecola della glicoforina contiene soltanto però residui amminoacidi idrofobici, da queste osservazioni sperimentali è derivata l’organizzazione molecolare della glicoforina sotto riportata.
I domini carbossiterminali e amminoterminale contengono molti residui amminoacidici polari o carchi e sono quindi relativamente idrofilici; un lungo segmento al centro della molecola della glicoforina contiene soltanto però residui amminoacidi idrofobici, da queste osservazioni sperimentali è derivata l’organizzazione molecolare della glicoforina sotto riportata. Lo scambiatore cloruro-bicarbonato della membrana dell’eritrocita consente l’ingresso o l’uscita della HCO 3-senza variazioni nel potenziale elettrico transmembrana. La funzione di questo sistema di trasporto è quello di aumentare la capacità di trasporto della CO 2nel sangue.
Lo scambiatore cloruro-bicarbonato della membrana dell’eritrocita consente l’ingresso o l’uscita della HCO 3-senza variazioni nel potenziale elettrico transmembrana. La funzione di questo sistema di trasporto è quello di aumentare la capacità di trasporto della CO 2nel sangue.
 Il processo inizia con il legame di tre ioni Na +a siti ad alta affinità sulla subunità più grande della proteina trasportatrice sulla superficie interna della membrana. (a) la stessa parte della subunità più grande possiede anche un sito che lega l’ATP.
Il processo inizia con il legame di tre ioni Na +a siti ad alta affinità sulla subunità più grande della proteina trasportatrice sulla superficie interna della membrana. (a) la stessa parte della subunità più grande possiede anche un sito che lega l’ATP. Le due catene polipeptidiche della spettrina sono disposte parallelamente e variamente avvolte l’una intorno all’altra a formare dimeri flessibili.
Le due catene polipeptidiche della spettrina sono disposte parallelamente e variamente avvolte l’una intorno all’altra a formare dimeri flessibili.
 è formata da due catene alfa e due delta, l’emoglobina F (HbF) trovata ne feto e nei primi periodi di vita postnatale,
è formata da due catene alfa e due delta, l’emoglobina F (HbF) trovata ne feto e nei primi periodi di vita postnatale,
 A): eritrocito che mostra il profilo biconcavo e il contenuto omogeneamente denso; B): neutrofilo che mostra il nucleo polilobulato che in sezione appare come profili nucleari separati; C): Eosinofilo, che mostra granulazioni specifiche con inclusioni cristalline; D): monocito che mostra una incisura nucleare, un reticolo endoplasmatico e dei lisosomi; E): piccolo linfocito; F): un gruppo di piastrine.
A): eritrocito che mostra il profilo biconcavo e il contenuto omogeneamente denso; B): neutrofilo che mostra il nucleo polilobulato che in sezione appare come profili nucleari separati; C): Eosinofilo, che mostra granulazioni specifiche con inclusioni cristalline; D): monocito che mostra una incisura nucleare, un reticolo endoplasmatico e dei lisosomi; E): piccolo linfocito; F): un gruppo di piastrine.



 Disegno schematico dell’ultrastruttura di un neurone somatico, che ne mostra il perinofero e parte dell’albero dendritico (in alto, a sinistra); i dendriti sono coperti di spine, in contatto con tipi differenti di terminali sinaptici.
Disegno schematico dell’ultrastruttura di un neurone somatico, che ne mostra il perinofero e parte dell’albero dendritico (in alto, a sinistra); i dendriti sono coperti di spine, in contatto con tipi differenti di terminali sinaptici.

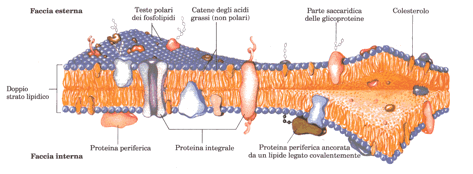
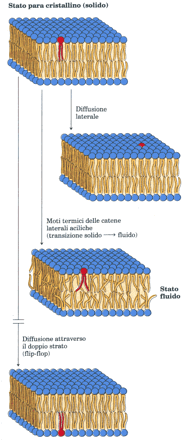 esse hanno movimenti di diffusione laterale così veloci che una molecola di lioide può circumnavigare un eritrocita in pochi secondi.
esse hanno movimenti di diffusione laterale così veloci che una molecola di lioide può circumnavigare un eritrocita in pochi secondi.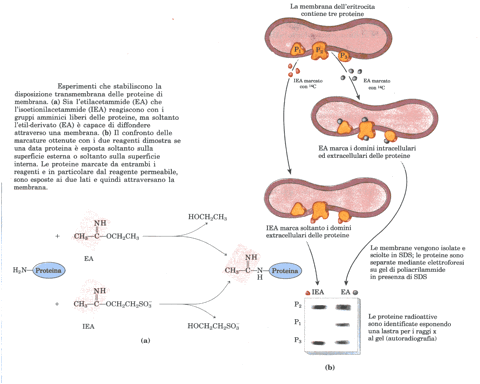
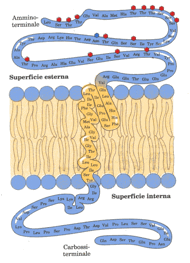 Un dominio idrofilico, contenete tutti i residui saccaridici, è sulla superficie esterna e un altro domino idrofilico è sulla superficie interna. Gli esagoni rappresentano unità tetrasaccaridiche (contenenti due NeuNAc, Gal e GalNAc) legate con un legame O-glicosidici a residui di serina o di treonina della proteina; l’esagono in blu rappresenta un oligosaccaride legato con un legame N-glicosidico a un residuo di asparagina. Un segmento composto da residui relativamente idrofobici forma una α elica che attraversa il doppio strato lipidico.
Un dominio idrofilico, contenete tutti i residui saccaridici, è sulla superficie esterna e un altro domino idrofilico è sulla superficie interna. Gli esagoni rappresentano unità tetrasaccaridiche (contenenti due NeuNAc, Gal e GalNAc) legate con un legame O-glicosidici a residui di serina o di treonina della proteina; l’esagono in blu rappresenta un oligosaccaride legato con un legame N-glicosidico a un residuo di asparagina. Un segmento composto da residui relativamente idrofobici forma una α elica che attraversa il doppio strato lipidico. Lo scambiatore cloruro-bicarbonato della membrana dell’eritrocita consente l’ingresso o l’uscita della HCO-3 senza variazioni nel potenziale elettrico transmembrana.
Lo scambiatore cloruro-bicarbonato della membrana dell’eritrocita consente l’ingresso o l’uscita della HCO-3 senza variazioni nel potenziale elettrico transmembrana.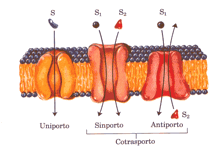 Le tre classi di sistema di trasporto differiscono nel numero di soluti (substrati) trasportati e nella direzione in cui ogni substrato viene trasportato; questa classificazione non tiene conto della eventuale richiesta di energia del sistema (trasporto attivo) o della su dipendenza energetica (trasporto passivo.
Le tre classi di sistema di trasporto differiscono nel numero di soluti (substrati) trasportati e nella direzione in cui ogni substrato viene trasportato; questa classificazione non tiene conto della eventuale richiesta di energia del sistema (trasporto attivo) o della su dipendenza energetica (trasporto passivo.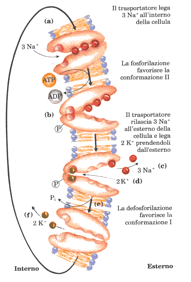 Il processo inizia con il legame di tre ioni Na+ a siti ad alta affinità sulla subunità più grande della proteina trasportatrice sulla superficie interna della membrana. (a) la stessa parte della subunità più grande possiede anche un sito che lega l’ATP.
Il processo inizia con il legame di tre ioni Na+ a siti ad alta affinità sulla subunità più grande della proteina trasportatrice sulla superficie interna della membrana. (a) la stessa parte della subunità più grande possiede anche un sito che lega l’ATP.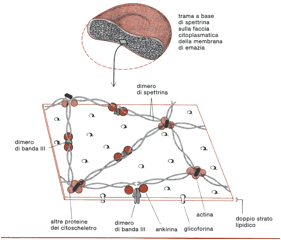 Le due catene polipeptidiche della spettrina sono disposte parallelamente e variamente avvolte l’una intorno all’altra a formare dimeri flessibili.
Le due catene polipeptidiche della spettrina sono disposte parallelamente e variamente avvolte l’una intorno all’altra a formare dimeri flessibili. È una proteina globulare con un peso molecolare di 67.000, composta da molecole di globina legate all’eme, che contiene, a sua volta, un gruppo profirinico contenente ferro. Ogni molecola è costituita da quattro subunità: ognuna delle quali è a sua volta costituita da una catena polipeptidica avvolta a spirale con una fessura che contiene un singolo gruppo eme; nel sangue degli individui normali si possono trovare quattro catene polipeptidiche chiamate alfa, beta, gamma e delta. L’emoglobina A (HbA), che nell’adulto rappresenta la classe maggiore, contiene due catene alfa e due beta; l’emoglobina A2 (HbA2), presente in una minore percentuale di adulti, è formata da due catene alfa e due delta, l’emoglobina F (HbF) trovata ne feto e nei primi periodi di vita postnatale, consta di due catene alfa e due gamma. Nelle condizioni patologiche della thalassemia viene sintetizzato soltanto un tipo di catena, in modo tale che una molecola possa contenere quattro catene alfa (b-thalassemia) o, più comunemente, quattro catene beta (a-thalassemia).
È una proteina globulare con un peso molecolare di 67.000, composta da molecole di globina legate all’eme, che contiene, a sua volta, un gruppo profirinico contenente ferro. Ogni molecola è costituita da quattro subunità: ognuna delle quali è a sua volta costituita da una catena polipeptidica avvolta a spirale con una fessura che contiene un singolo gruppo eme; nel sangue degli individui normali si possono trovare quattro catene polipeptidiche chiamate alfa, beta, gamma e delta. L’emoglobina A (HbA), che nell’adulto rappresenta la classe maggiore, contiene due catene alfa e due beta; l’emoglobina A2 (HbA2), presente in una minore percentuale di adulti, è formata da due catene alfa e due delta, l’emoglobina F (HbF) trovata ne feto e nei primi periodi di vita postnatale, consta di due catene alfa e due gamma. Nelle condizioni patologiche della thalassemia viene sintetizzato soltanto un tipo di catena, in modo tale che una molecola possa contenere quattro catene alfa (b-thalassemia) o, più comunemente, quattro catene beta (a-thalassemia).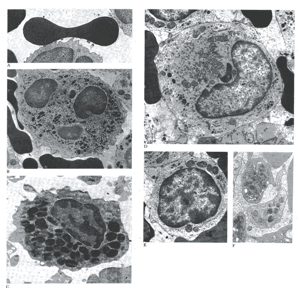

 Gli enzimi sono macromolecole proteiche in cui la struttura conformazionale è depositaria di “memorie”, interattive con i substrati specifici, gli Enzimologi “classici” consideravano il sito attivo dell’ enzima come una struttura rigida e l’adattamento di un substrato nel sito attivo più o meno come quello di una chiave nella serratura (analogia suggerita per la prima volta nel 1894 dal biochimico tedesco Emil Fischer).
Gli enzimi sono macromolecole proteiche in cui la struttura conformazionale è depositaria di “memorie”, interattive con i substrati specifici, gli Enzimologi “classici” consideravano il sito attivo dell’ enzima come una struttura rigida e l’adattamento di un substrato nel sito attivo più o meno come quello di una chiave nella serratura (analogia suggerita per la prima volta nel 1894 dal biochimico tedesco Emil Fischer).

 RICONOSCIMENTO DI ESECUZIONE LAVORI
RICONOSCIMENTO DI ESECUZIONE LAVORI